28 de Maio de 2021
Biofilmes na indústria alimentar
O que são os biofilmes?
Biofilmes são estruturas complexas formadas por microrganismos que se fixam firmemente a uma superfície através de uma matriz extracelular (conhecida como EPS "extracelular polymeric substance"), gerada por secreções dos próprios microrganismos e composta principalmente por polissacarídeos, proteínas, lipídos e ADNe (ADN extracelular). A criação da matriz EPS envolve um custo energético muito elevado, o que é amplamente justificado pelas vantagens evolutivas que confere ao sistema, conferindo-lhe, entre outras, as seguintes propriedades [1]:- Resistência à dissecação.
- Resistência a certos antibióticos.
- Resistência a desinfetantes, tanto à base de tensioativos, como de poder oxidante.
- Resistência à luz UV.
- Disponibilidade de nutrientes.
- Troca horizontal de material genético.
- Os polissacarídeos solúveis conferem-lhe uma consistência gelatinosa e desempenham um papel importante na retenção e disponibilidade de água.
- Os polissacarídeos insolúveis, maiores, fornecem rigidez estrutural.
- As proteínas e enzimas intervêm na digestão de macromoléculas e na disponibilidade de nutrientes.
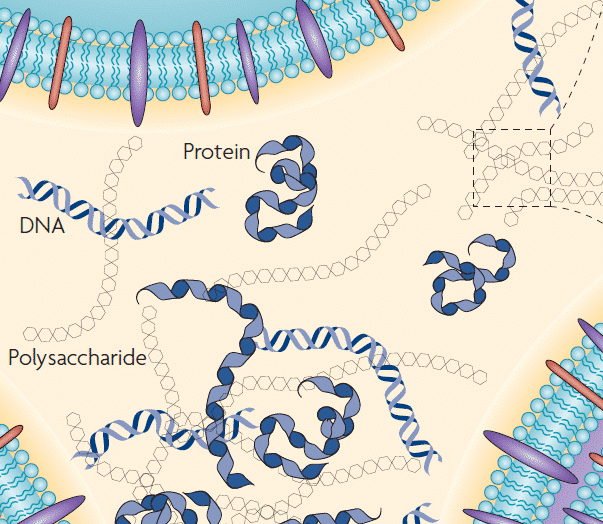
| ©Flemming & Wingender |
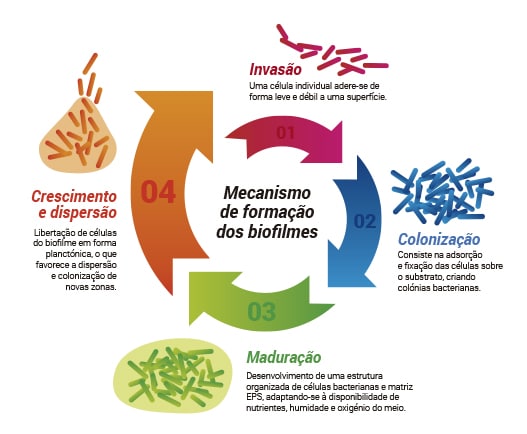
Mecanismo de formação dos biofilmes
A formação de biofilmes é um processo amplamente conhecido em termos gerais, embora ainda seja objeto de estudo para aprofundar os mecanismos específicos que o compõem. O processo começa quando as células plantónicas começam a aderir a uma superfície (metálica, plástica, ...) e a segregar substâncias viscosas (EPS) que favorecem a aderência e a coesão, ao mesmo tempo que promovem o crescimento e a incorporação de novos microrganismos ao sistema. O mecanismo de formação dos biofilmes, de forma geral, pode ser dividido nas seguintes quatro etapas:- Invasão - Nesta fase, as células plantónicas começam a aderir debilmente à superfície. A deposição por gravidade e a ancoragem favorecidas pela morfologia da superfície e pela presença de resíduos são os mecanismos de aderência mais comuns.
- Colonização - Forças de atração eletrostáticas e estruturas celulares como flagelos, fímbiras e pili são os tipos de aderência mais comuns nos estágios iniciais desta fase. Esta primeira adsorção é relativamente fácil de reverter, as forças de Van der Waals e a atração eletrostática podem ser superadas pela repulsão natural causada pela carga negativa da membrana celular em contato com a superfície (geralmente carregada negativamente), algumas das células colonizadoras podem voltar a separar-se do substrato.
- Maturação - Após um tempo de latência inicial, os microrganismos começam a dividir-se, crescendo em direção ao topo do biofilme em estruturas tipicamente em forma de cogumelo. Os biofilmes podem atingir altos níveis de complexidade, criando sistemas eficientes de distribuição de nutrientes e atingindo níveis de estratificação que permitem o crescimento de espécies anaeróbias em ambientes com presença de oxigénio graças à proteção de uma camada aeróbia. Diferentes espécies formadoras de biofilme podem colaborar entre si, trocando material genético, sintetizando enzimas e proteínas específicas e criando gradientes que favorecem seu crescimento.
- Crescimento e dispersão - Nesta fase, células são libertadas para o ambiente que retornam à sua forma plantónica e que, cumpridas as condições necessárias, podem originar novos focos de formação de biofilme. A duração desta fase, e do biofilme em geral, será determinada pela disponibilidade de nutrientes e pelo cumprimento das condições necessárias à sua sobrevivência.
 Fatores que favorecem o desenvolvimento de biofilmes.
Os principais fatores que intervêm no desenvolvimento de um biofilme podem ser classificados em:
Fatores que favorecem o desenvolvimento de biofilmes.
Os principais fatores que intervêm no desenvolvimento de um biofilme podem ser classificados em:
- Microrganismos - O tipo e diversidade de espécies que compõem o biofilme, bem como as concentrações iniciais e sua viabilidade, podem marcar as hipóteses de sucesso na sua formação e na sua permanência na superfície.
- Características do substrato - Qualquer tipo de superfície que reúna as condições necessárias de humidade e disponibilidade de nutrientes, é suscetível de ser um ponto de formação de biofilme. No entanto, as características inerentes à sua composição e ao seu estado geral de manutenção (rachas, desgaste, ...) podem influenciar significativamente a facilidade com que os microrganismos presentes no meio podem aderir e, portanto, aumentar a possibilidade de formação de biofilme. Por exemplo, superfícies de plástico como teflon, correias transportadoras, mesas de corte ou juntas poliméricas representam um risco maior do que superfícies de metal como mesas, bancadas, lâminas ou circuitos.
- Condições ambientais - Os microrganismos devem ter, pelo menos nas fases iniciais de formação do biofilme, as condições de temperatura, humidade e disponibilidade de nutrientes necessárias ao seu crescimento. Estas condições podem variar ligeiramente em função das espécies formadoras, mas em geral coincidem com as condições de humidade e disponibilidade de nutrientes que encontramos na maioria dos processos da indústria alimentar.
Consequências da formação de biofilmes
As consequências da formação do biofilme variam de acordo com o sistema ou processo afeto, o que pode causar problemas significativos de segurança alimentar e gerar elevados custos tecnológicos. Na indústria alimentar, os biofilmes são a causa de alterações organoléticas e contaminação microbiológica de produtos processados, atuando como um reservatório perfeito para microrganismos patogénicos como Listeria, Salmonella e Escherichia Coli, entre outros. Interiores de circuitos, tubagens de água, bicos doseadores, mesas e teflon são apenas alguns dos exemplos de superfícies da indústria alimentar onde podemos encontrar biofilme. Os biofilmes podem formar-se rapidamente em ambientes industriais, sendo também a causa de vários outros problemas como corrosão de equipamentos e instalações, obstrução de tubagens ou diminuição do desempenho de instalações, como trocadores de calor ou sistemas de filtração. La matriz extracelular que forma el biofilm actúa como protector de las bacterias y barrera de difusión física y química, lo que dificulta la penetración de agentes antimicrobianos, imposibilitando una correcta actuación de los protocolos de limpieza y desinfección. Adicionalmente, también aumentan los mecanismos de resistencia de los microorganismos, que se adaptan al nuevo entorno que genera el biofilm. Unas deficientes condiciones higiénicas en las superficies alimentarias aumentan significativamente las posibilidades de desarrollo de biofilmes, debido a las características de la biocapa formada:- Velocidade rápida de formação de biofilme (apenas algumas horas em condições favoráveis).
- Capacidade de propagação e recolonização.
- Resistência aos processos de limpeza e desinfeção (os biofilmes podem ser entre 10 e 100 vezes mais resistentes do que as bactérias em suspensão).
- Crescimento em áreas de difícil acesso (pontos críticos).
- Dificuldade de amostragem, deteção (tamanho microscópico) e controlo.
Pretende mais informações?
Contacte-nos.
De acordo com o Regulamento 2016/679 (GDPR), fornecemos-lhe informação básica sobre proteção de dados pessoais:
-Responsável pelo tratamento: PROQUIMIA, S.A.
-Finalidade do tratamento: Gerir o envio de informação, resolver consultas e/ou recolher dados para possíveis relações comerciais.
-Legitimação: Consentimento do titular dos dados
-Destinatários: Não serão cedidos dados a terceiros, salvo por obrigação legal.
-Direitos: Acesso, retificação, eliminação, oposição, limitação, portabilidade e apresentação de queixas.
-Informações adicionais: pode consultar informações adicionais e detalhadas sobre Proteção de Dados no nosso site: Política de privacidade



