1 de abril de 2022
Listeriosis
 La Listeriosis es una infección causada por la bacteria Listeria monocytogenes. Los brotes de esta enfermedad se relacionan generalmente con la ingesta de alimentos que contienen gran cantidad de esta bacteria.
Se trata de una enfermedad relativamente poco frecuente, ya que su incidencia es bastante baja en comparación con otras enfermedades asociadas a microorganismos transmitidos por los alimentos.
Sin embargo, la Listeriosis es motivo de especial interés y preocupación ya que en su forma invasiva es una enfermedad grave, con tasas de letalidad muy elevadas (entre el 10% y el 30%). Y es que Listeria monocytogenes es un patógeno oportunista que casi siempre afecta a la población de riesgo, mientras que en la población general su infección no suele conllevar desarrollo de la enfermedad.
La Listeriosis es una infección causada por la bacteria Listeria monocytogenes. Los brotes de esta enfermedad se relacionan generalmente con la ingesta de alimentos que contienen gran cantidad de esta bacteria.
Se trata de una enfermedad relativamente poco frecuente, ya que su incidencia es bastante baja en comparación con otras enfermedades asociadas a microorganismos transmitidos por los alimentos.
Sin embargo, la Listeriosis es motivo de especial interés y preocupación ya que en su forma invasiva es una enfermedad grave, con tasas de letalidad muy elevadas (entre el 10% y el 30%). Y es que Listeria monocytogenes es un patógeno oportunista que casi siempre afecta a la población de riesgo, mientras que en la población general su infección no suele conllevar desarrollo de la enfermedad.
Grupos de riesgo:- Mujeres embarazadas - Recién nacidos - Personas con las defensas debilitadas: o Enfermos crónicos o Personas de edad avanzada o Personas sometidas a determinados tratamientos médicos · La probabilidad de contraer la enfermedad es unas 20 veces mayor en las embarazadas que en otros adultos sanos. · Los pacientes con VIH/sida tienen una probabilidad 300 veces mayor de sufrir listeriosis que las personas con un sistema inmunitario normal. · Personas mayores de 65 años representan un 62% de los afectados totales, con una mortalidad del 19%. |
Incidencia de la Listeriosis
La tasa de Listeriosis humana en la Unión Europea en 2019 tiene un Prevalencia de 0,46 casos por cada 100.000 habitantes (EFSA 2020). En España no se dispone todavía del dato de 2019, pero la tasa en 2018 fue de casi el doble de este valor, situándose en 0,89 casos por cada 100.000 habitantes (EFSA 2019). La tendencia en la UE de casos confirmados de Listeriosis se mantuvo estable en los tres últimos años (2621 casos en 2019).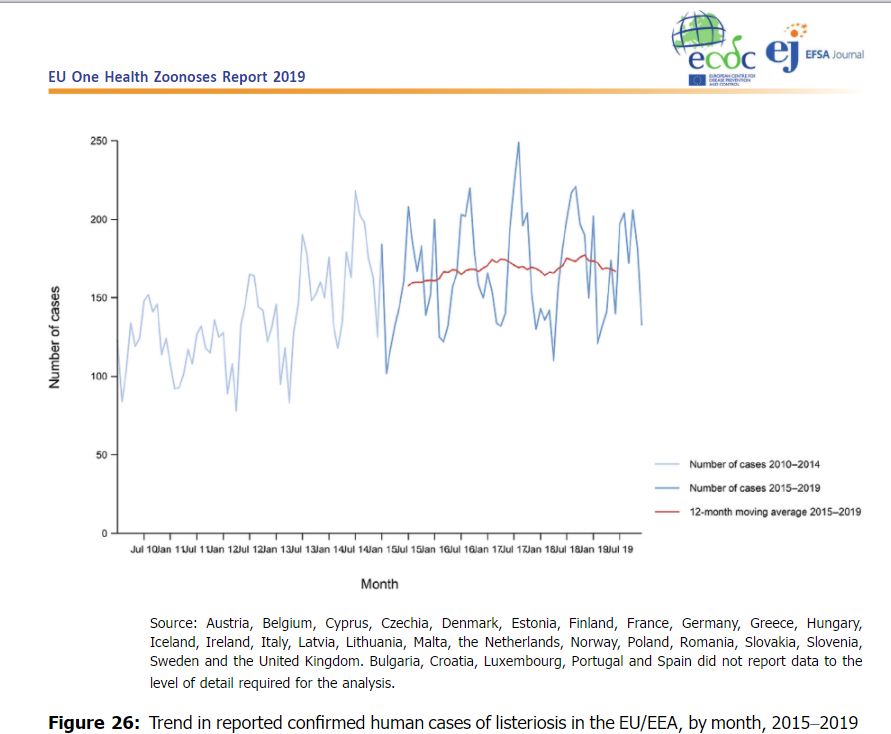 Trend in reported confirmed human cases of listeriosis in the EU/EEA, by month, 2009– 2019
Por otro lado, los datos mundiales (OMS 2018) muestran poca prevalencia (0,01-0,1 casos por cada 100.000 personas) pero una muy alta mortalidad (20 – 30%) en personas sensibles.
Trend in reported confirmed human cases of listeriosis in the EU/EEA, by month, 2009– 2019
Por otro lado, los datos mundiales (OMS 2018) muestran poca prevalencia (0,01-0,1 casos por cada 100.000 personas) pero una muy alta mortalidad (20 – 30%) en personas sensibles.
Dosis infectiva
La dosis infectiva no está determinada y depende de factores como la cepa, la susceptibilidad del huésped (estado inmunitario, edad,…) o la matriz alimentaria involucrada. Según un modelo utilizado por la EFSA, el 92% de los casos de Listeriosis invasiva serían atribuibles a dosis superiores a 100.000 unidades formadoras de colonias (UFC) por porción. Por lo tanto, si suponemos un tamaño promedio de porción de 50 g, esto correspondería a una concentración de Listeria monocytogenes por encima de 2.000 UFC/g en el momento del consumo. De todas formas, es probable que menos de 1.000 UFC/g puedan causar enfermedad en individuos susceptibles.Período de incubación
La gastroenteritis causada por Listeria monocytogenes tiene un período de incubación relativamente corto, que va desde unas pocas horas hasta 2 o 3 días. Por otro lado, en la forma grave e invasiva de la enfermedad, el periodo de incubación suele ser de 1 a 2 semanas, pero puede oscilar entre algunos días y 3 meses. Este prolongado periodo de incubación hace que resulte difícil identificar el alimento que está en el origen de la infección.Síntomas
La Listeriosis causa dos formas de enfermedad en los seres humanos:- No invasiva: es una forma leve que afecta sobre todo a personas sanas. Los síntomas son diarrea, fiebre, dolor de cabeza y dolores musculares.
- Invasiva: es más grave y afecta a los grupos de alto riesgo. Se caracteriza por síntomas graves y una alta tasa de mortalidad (20-30%). Entre sus síntomas se encuentran la fiebre, los dolores musculares, la septicemia y la meningitis.
Tratamiento
La Listeriosis se puede tratar si se diagnostica a tiempo. Los antibióticos se utilizan para tratar síntomas graves como la meningitis. Cuando se produce una infección durante el embarazo, la administración inmediata de antibióticos previene la infección del feto o del recién nacido.Transmisión
Listeria monocytogenes se puede transmitir a las personas por vía vertical (madre-hijo a través de la placenta), zoonótica y/o nosocomial. Actualmente, el 99% de los casos de Listeriosis humana son de transmisión alimentaria a través del consumo de alimentos de origen animal (carne, pescado, leche, etc.) contaminados con patógenos.¿Cómo prevenir la listeriosis?
En general, la prevención de la Listeriosis es similar a la prevención de otras enfermedades transmitidas por alimentos y, por tal motivo, es importante seguir las cinco claves para la inocuidad de los alimentos definidas por la OMS:- Mantenga la limpieza.
- Separe alimentos crudos y cocinados.
- Cocine completamente:
- Los grupos de riesgo tienen que conocer los alimentos de riesgo y evitar su consumo o consumirlos previo tratamiento térmico a más de 70°C.
- Mantenga los alimentos a temperaturas seguras:
- Mantener siempre la temperatura de la nevera por debajo de los 4°C.
- Use agua y materias primas seguras:
- Respetar las fechas de caducidad de los alimentos que se mantienen refrigerados.
- Evitar consumir productos lácteos elaborados con leche no pasteurizada; fiambres y productos cárnicos listos para el consumo como salchichas, jamones, patés y carnes para untar, así como mariscos ahumados en frío (como salmón ahumado);
- Respetar la vida útil y la temperatura de almacenamiento escritas en las etiquetas de los alimentos listos para el consumo;
- Cocinar antes de comer es otra forma muy eficaz de matar las bacterias.
- La Listeriosis es una enfermedad relativamente poco frecuente pero su forma invasiva es una enfermedad grave, con altas tasas de letalidad sobretodo en los grupos de riesgo.
- Su dosis infectiva no está completamente determinada y su periodo de incubación puede variar des de unas horas a casi 3 meses.
- Para prevenir la enfermedad, deberíamos conocer los alimentos de riesgo y seguir las cinco claves para la inocuidad de los alimentos propuestas por la OMS.
Fuentes
- Boletín acsa brief nº9 mayo-junio 2018. 2018. https://bit.ly/2Sc0jt3
- Publicado el informe de la UE sobre las zoonosis “One Health” 2019. 2021. https://bit.ly/3vyuFqS
- EFSA Journal. The European Union One Health 2018 Zoonoses Report. 2019. https://bit.ly/34XukE8
- EFSA Journal. The European Union One Health 2019 Zoonoses Report. 2021. https://bit.ly/3wIRPw0
- Informe One Health sobre Zoonosis en Europa 2019. 2021. https://bit.ly/3iMRdl3
- Listeria. https://bit.ly/2HFPZaJ
- Listeriosis. 2018. https://bit.ly/3xkCfGW
¿Quieres más información?
Te ayudamos
De acuerdo con el Reglamento (UE) 2016/679, General de Protección de Datos (RGPD), le facilitamos la información básica sobre el tratamiento de sus datos personales:
- Responsable del tratamiento: PROQUIMIA, S.A.
- Finalidad del tratamiento: Gestionar el envío de información, la resolución de consultas y/o la recogida de datos para posibles relaciones comerciales.
- Legitimación: Consentimiento del interesado.
- Destinatarios: No se cederán datos a terceros, salvo obligación legal.
- Derechos: Tiene derecho a acceder, rectificar y suprimir los datos, así como a otros derechos, como se explica en la información adicional.
- Información adicional: Puede consultar la información adicional y detallada sobre protección de datos en nuestra página web, en la sección: Política de privacidad


